La Comisión Europea ha permitido la comercialización de Komboglyzetm, un medicamento para los adultos con diabetes tipo II, según han anunciado este miércoles los laboratorios farmacéuticos Bristol-Myers Squibb y AstraZeneca.
La Comisión Europea ha permitido la comercialización de Komboglyzetm, un medicamento para los adultos con diabetes tipo II, según han anunciado este miércoles los laboratorios farmacéuticos Bristol-Myers Squibb y AstraZeneca.
La saxagliptina y la metformina hidrocloruro de liberación inmediata y combinación fija está indicada, junto con la dieta y el ejercicio, para mejorar el control glucémico.
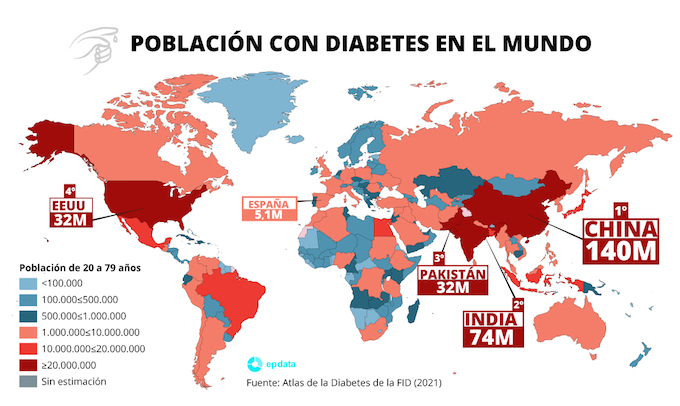
La diabetes tipo II afecta a cerca de 53 millones de personas de entre 20 y 79 años en Europa y se espera que esta cifra aumente a más de 64 millones en 2030, han señalado las farmacéuticas.
Estos enfermos de los 27 países miembros de la Unión Europea podrán desde ahora tomar Komboglyzetm, un fármaco que combina en un comprimido la saxagliptina -un inhibidor de la DPP-4- y metformina de liberación inmediata, una biguanida.
El medicamento está especificado además para pacientes no controlados adecuadamente con la dosis máxima tolerada de metformina sola o que están recibiendo ya tratamiento con la combinación de saxagliptina y metformina en comprimidos distintos.
Para conseguir la aprobación de la Unión Europea se ha realizado un estudio sobre 4.326 pacientes, de los que 2.158 recibieron saxagliptina más metformina. Tras ello, la bioequivalencia de Komboglizetm con la administración de saxagliptina y metformina fue demostrada en estudios adicionales.